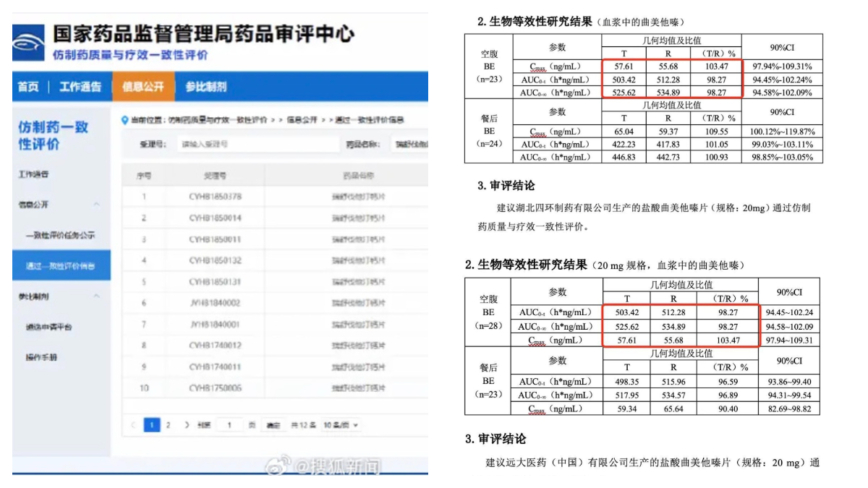
【新唐人北京时间2025年01月26日讯】近日,大陆集采药问题成为舆论关注焦点。有医生提出,集采药一致性评价数据出现罕见雷同。中共药监局声称是编辑错误,并关闭数据下载,引发了更大质疑。
陆媒1月25日报导,中共国家药物监督管理局回应称“数据雷同是编辑错误”之后,外界已无法从国家药监局官网下载一致性评价数据。
报导说,公众的质疑没有因上述说明而停止。例如,有质疑指出,两款盐酸曲美他嗪片的一致性评价试验相隔两年之久,不太可能因连续处理两份文件导致数据编辑错误,而且数据顺序也有人为调整痕迹。
又例如,药审中心对数据进行了“更正”。然而,有网友通过简单的计算发现,“修正”后的数据仍然存在疑点。在Lek Pharmaceutical瑞舒伐他汀钙片生物等效性研究结果的餐后BE血药浓度(AUC)指标中,测试样本T值与对照品R值同为74.3,却得出了(T/R)比值为98.95%,而非100%。
报导指出,如果数据雷同是编辑问题,药监局应详细解释一致性评价数据的收集上传流程是怎样的。是药企将原始数据上报后,药监局从数据包中摘取对应数据,还是药企上传的文件本就是目前公开的模板,又或者是药监局专家去企业现场核查后自行汇总数据?
药监局还应公开数据雷同的3款药物的原始试验数据。这些样本当然是脱敏的,样本量也并不大,基本在20多例。依据这些原始数据,公众可以按照科学的统计方法,对比药监局已公开的生物等效性研究结果,自然可得出公正的结论。
报导质问:“为何关闭一致性评价数据下载权限?”
1月25日,微信公众号“建设性意见”发文《药监局说数据雷同是编辑错误,我有3点不认同》。文章指出,此前曝光的关于两个厂家瑞舒伐他汀钙片生物等效性试验数据完全一致的情况,用编辑错误是可以解释的。经常编辑表格的人可以理解,处理类似文件时套用模板时,不小心把A文件的数据当成了B文件的数据,是可能的。
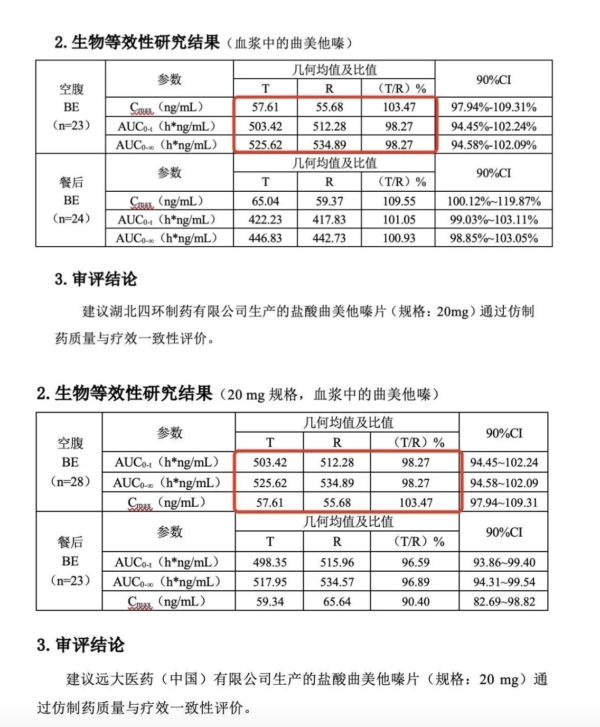
但是,关于盐酸曲美他嗪片的数据雷同,却无法用编辑错误搪塞。原因有三个,第一,数据顺序有人为调整痕迹。仔细观察两个表格可以发现,第一个表格的三行数据排列是123,而第二个表格的三行数据排列是231,也就是人为把第1行数据剪切后黏贴到了第三行;
第二,数据一半雷同一半不同。两组表格里,空腹试验的数据完全一致,到了餐后试验的数据却又出现了明显不同。这更进一步表明,不太可能是因为整体复制黏贴导致的错误;
第三,两份数据相隔两年之久。从两份文件中的试验编号可以看到,上述两项研究分别发生在2019年和2017年。以常理推断,不太可能是因为连续处理这两份文件导致的编辑错误。
文章指出,“更大的可能是,处理2019年文件时从此前的多份同品种药品数据中分别摘录了一些数据来填充,为了避免完全雷同,操作者对数据顺序做了手动调整。”
文章最后呼吁,“把更多原始数据公开出来,真相自会浮现,流言自会终结。”
但是,文章说,自己和朋友1月24日晚上9点访问药监局网站时,发现药品一致性评价相关的全部公开文件已经无法下载。
1月24日,微信公众号“夏志敏医生”发布题为《仿制药一致性评价大量数据雷同》的文章指出,中共药监局网站上,出现仿制药一致性评价数据雷同,引发热议。之后,中共药监局审评中心紧急“修改”了数据,并发布声明称“个别数据重复系编辑错误”。
(记者李郦综合报导/责任编辑:云涛)